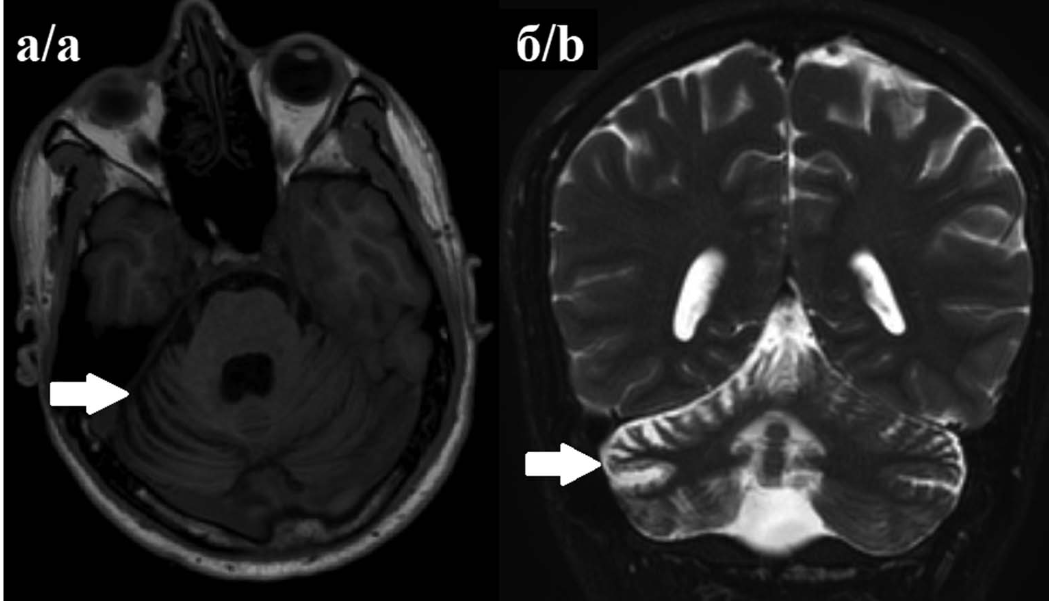
Паранеопластическая мозжечковая дегенерация
Паранеопласти́ческая мозжечко́вая дегенера́ция (ПМД) — это аутоиммунное заболевание центральной нервной системы и наиболее распространённый паранеопластический синдром с поражением головного мозга. В основе патологии лежит преимущественное повреждение клеток Пуркинье мозжечка, приводящее к тяжёлой мозжечковой дисфункции. Заболевание характеризуется быстрым, подострым началом с доминирующим симптомом атаксии, которая в течение нескольких недель или месяцев прогрессирует до полной утраты способности к самостоятельному передвижению. Клиническая картина часто также включает дизартрию, нарушение движений глаз в виде саккад и нистагм[1][2].
История[править]
Впервые данное заболевание было описано в 1919 году Бернардом Браувером, однако его концепция получила широкое признание только через девятнадцать лет. В 1938 году совместная работа Бернарда Браувера и Алберта Бимонда, описавшая связь дегенеративных мозжечковых изменений с онкологической патологией яичников, стала ключевым подтверждением первоначальной теории[2].
Классификация[править]
ПМД относится к паранеопластическим неврологическим синдромам[3].
Этиология[править]
В основе ПМД лежит аутоиммунный процесс, запускаемый наличием злокачественного опухолевого процесса. Заболевание наиболее часто ассоциировано с определёнными типами опухолей: раком молочной железы, раком яичников, мелкоклеточным раком лёгкого и лимфомой Ходжкина. Описано более тридцати видов патогенных антинейрональных антител, из которых в клинической практике наиболее часто выявляются антитела к Yo-1 (также известные как PCA-1)[3].
Патогенез[править]
ПМД представляет собой воспалительный аутоиммунный процесс, при котором происходит разрушение клеток Пуркинье мозжечка. Механизм заболевания связан с выработкой иммунной системой онконевральных антител в ответ на белок, экспрессируемый опухолевыми клетками, известный как белок 2, ассоциированный с дегенерацией мозжечка. Данные антитела перекрёстно реагируют со схожим белком, присутствующим в клетках Пуркинье, что приводит к их гибели. Патологический процесс часто начинается локально, но постепенно распространяется на весь мозжечок, также отмечается вовлечение структур ствола мозга. Скорость развития повреждения варьируется у разных пациентов: от острого начала симптомов до более подострого, медленно прогрессирующего течения[4].
У пациентов с ПМД выявляется широкий спектр патогенных онконевральных антител, к которым относятся анти-Yo (PCA-1), анти-Hu, анти-Ri, анти-Tr, анти-VGCC, анти-Ma, анти-CRMP5 (анти-CV2) и анти-mGluR. Наиболее часто обнаруживаемыми являются анти-Yo антитела (также известные как антитела к цитоплазме клеток Пуркинье 1-го типа), которые обычно ассоциированы с раком молочной железы и гинекологическими злокачественными новообразованиями[4].
Основным гистологическим признаком ПМД является выраженная диффузная потеря клеток Пуркинье по всей коре мозжечка. В исследуемых образцах эти клетки полностью отсутствуют. Потеря других типов клеток наблюдается, но является редкой. В некоторых случаях утрата клеток Пуркинье носит очаговый характер. Также отмечаются воспалительные изменения, проявляющиеся лимфоцитарной инфильтрацией. Наблюдается атрофия зернистого и молекулярного слоёв мозжечка с пролиферацией микроглии и астроцитозом, в то время как корзинчатые клетки остаются относительно сохранными. Глубокие ядра мозжечка и его связи со стволом мозга, как правило, не поражены. У пациентов с антителами aанти-Yo обычно наблюдаются более выраженные воспалительные изменения и характерная картина иммунофлюоресценции, при которой выявляется грубогранулярное окрашивание цитоплазмы клеток Пуркинье, а также их проксимальных аксонов и дендритов; ядра клеток и системные ткани при этом не окрашиваются. При ПМД, связанной с антителами aнти-Hu, окрашиванию подвергаются ядра нейронов коры мозжечка[5].
Эпидемиология[править]
ПМД является крайне редким заболеванием, которое, по оценкам, развивается менее чем у одного процента онкологических пациентов. В связи с редкостью данного синдрома доступные эпидемиологические данные ограничены. Предполагается, что ПМД встречается чаще у женщин[4].
Диагностика[править]
Клиническая картина[править]
Пациенты с ПМД могут изначально предъявлять жалобы на слабо выраженные симптомы, такие как шаткость походки, двоение в глазах и затруднение при выполнении мелких движений кистями. Как правило, эти симптомы прогрессируют до развития атаксии в конечностях и туловищной атаксии. Также регистрируются признаки поражения ствола мозга, включая нистагм, дизартрию и дисфагию. У части пациентов заболевание развивается медленно, в течение нескольких недель или месяцев, однако описаны случаи и быстрого нарастания симптоматики на протяжении дней. У некоторых больных двигательным нарушениям может предшествовать продромальный период, напоминающий гриппоподобное заболевание, с субфебрильной температурой, общим недомоганием, тошнотой и рвотой. Важно отметить, что мозжечковые симптомы нередко опережают диагностику основного злокачественного новообразования на срок от нескольких месяцев до нескольких лет[4].
Примерно у 20% пациентов с ПМД могут наблюдаться нарушения памяти и когнитивных функций, а также аффективные симптомы. Данный комплекс неврологических расстройств известен как мозжечковый когнитивно-аффективный синдром[5].
Инструментальные исследования[править]
Магнитно-резонансная томография головного мозга: картина обычно остаётся нормальной на ранних стадиях, однако в ряду случаев может определяться атрофия мозжечка[5].
Позитронно-эмиссионная томография с фтордезоксиглюкозой может быть использована для выявления первичного злокачественного новообразования, лежащего в основе синдрома[5].
С целью выявления первичной опухоли выполняется рентгенография органов грудной клетки, маммография и компьютерная томография органов брюшной полости или грудной клетки[5].
Лабораторные исследования[править]
Клинический анализ цереброспинальной жидкости: характерно выявление неспецифических изменений, такие как умеренный плеоцитоз, повышение концентрации белка или наличие олигоклональных полос. Однако эти находки не обладают достаточной чувствительностью или специфичностью для точной диагностики[4].
Иммуноферментный анализ крови[4]:
- анти-Yo (PCA-1): это наиболее часто выявляемые онконевральные антитела при паранеопластической мозжечковой дегенерации. Обычно ассоциированы с раком молочной железы и раком яичников;
- анти-Hu: часто связаны с мелкоклеточным раком лёгкого, раком предстательной железы и семиномой яичка;
- анти-Ri: ассоциированы с раком молочной железы, раком яичников и мелкоклеточным раком лёгкого;
- анти-Tr: связывают с лимфомой Ходжкина;
- анти-VGCC (к потенциал-зависимым кальциевым каналам): ассоциированы с мелкоклеточным раком лёгкого и лимфомой;
- анти-Ma2: ассоциированы с мелкоклеточным раком лёгкого и раком яичка;
- анти-CRMP5 (анти-CV2): связывают с мелкоклеточным раком лёгкого и тимомой;
- анти-mGluR1 (к метаботропному глутаматному рецептору 1 типа): ассоциированы с лимфомой Ходжкина.
Дифференциальная диагностика[править]
Также крайне важно проводить дифференциальную диагностику ПМД с другими неврологическими расстройствами, способными проявляться схожей клинической картиной. К ним относятся[4]:
- демиелинизирующие заболевания (например, рассеянный склероз);
- аутоиммунные заболевания, такие как мозжечковая дегенерация, ассоциированная с антителами к глутаматдекарбоксилазе, саркоидоз, системная красная волчанка и болезнь Бехчета;
- атипичные инфекции центральной нервной системы: болезнь Кройтцфельдта — Якоба, прогрессирующая мультифокальная лейкоэнцефалопатия;
- метаболические расстройства: дефицит витамина B12, алкогольная энцефалопатия Вернике, целиакия.
Осложнения[править]
Поздняя диагностика и несвоевременное начало лечения ПМД могут привести к тяжёлой инвалидизации пациента. Кроме того, отсрочка в выявлении первичной злокачественной опухоли, лежащей в основе синдрома, чревата прогрессированием онкологического заболевания, что влечёт за собой высокие риски осложнений и смерти[4].
Лечение[править]
Основные принципы лечения ПМД включают три направления: терапию ассоциированной злокачественной опухоли, иммуносупрессивная терапия и реабилитационные мероприятия. Наиболее эффективным подходом для стабилизации или улучшения неврологического состояния считается удаление первичной опухоли на ранних стадиях заболевания. Иммуносупрессивная терапия выступает в качестве важного дополнительного метода, эффективность которой варьируется в зависимости от иммунного механизма болезни. У пациентов с антителами против поверхностных или синаптических антигенов (гуморальный иммунитет) ответ на такое лечение, как правило, более выражен, чем у пациентов с антителами против внутриклеточных антигенов (T-клеточно-опосредованный иммунитет). Назначение иммуносупрессоров считается особенно целесообразным в случаях, когда опухоль не выявлена, или когда её лечение не привело к стабилизации неврологического дефицита[3].
В клинической практике применяются различные варианты иммунотерапии. К терапии первой линии относят глюкокортикостероиды, внутривенный иммуноглобулин и плазмаферез. При недостаточной эффективности переходят к терапии второй линии, включающей ритуксимаб и циклофосфамид, с возможностью их комбинации между собой и с препаратами первой линии. Несмотря на отсутствие убедительных доказательств превосходства какого-либо одного подхода, исследования показывают, что раннее начало иммуносупрессивного лечения (в течение первых трёх месяцев от дебюта симптомов) может улучшать клинический исход[3].
Прогноз[править]
ПМД имеет неблагоприятный прогноз. Симптомы у пациентов прогрессируют в течение недель или месяцев, и хотя у большинства больных состояние стабилизируется примерно через полгода от начала заболевания, к этому моменту они, как правило, уже имеют выраженную степень инвалидизации, будучи прикованными к инвалидному креслу или постели. Пациенты с анти-Yo и анти-Hu антителами имеют более тяжёлые симптомы, хуже отвечают на лечение и характеризуются более низкой общей выживаемостью по сравнению с пациентами, у которых выявляются анти-Tr и анти-Ri антитела[4].
Диспансерное наблюдение[править]
Пациенты с ПМД нуждаются в диспансерном наблюдении хирурга, онколога и невролога. Объём и частота диспансерных наблюдений определяется индивидуально[5].
Профилактика[править]
Не разработана.
Примечания[править]
- ↑ Королёва Е. С., Алифирова В. М., Рязанцева А. А., Кощавцева Ю. И. Паранеопластическая мозжечковая дегенерация у пациента с антителами anti-Yo и аденокарциномой простатырус. // Бюллетень сибирской медицины. — 2017. — том 16. — № 3. — С. 218-223. — DOI:10.20538/1682-0363-2017-3-218-223
- ↑ 2,0 2,1 Шнайдер Н. А., Ежикова В. В., Дыхно Ю. А., и др. Проблемы диагностики паранеопластической мозжечковой дегенерациирус. // Неврология, нейропсихиатрия, психосоматика. — 2014. — № 1. — С. 35-43.
- ↑ 3,0 3,1 3,2 3,3 Нужный Е. П., Краснов М. Ю., Москаленко А. Н., и др. Паранеопластическая мозжечковая дегенерациярус. // Российский неврологический журнал. — 2023. — том 28. — № 4. — С. 43-53. — DOI:10.30629/2658-7947-2023-28-4-43-53
- ↑ 4,0 4,1 4,2 4,3 4,4 4,5 4,6 4,7 4,8 Aly R., Emmady P. D. Paraneoplastic Cerebellar Degenerationанглийский. Statpearls (04.07.2023). Проверено 23 января 2026.
- ↑ 5,0 5,1 5,2 5,3 5,4 5,5 Lan R. Paraneoplastic Cerebellar Degenerationанглийский. Medscape (11/09/2024). Проверено 23/01/2026.
Литература[править]
- Ужный Е. П., Краснов М. Ю., Москаленко А. Н., и др. Паранеопластическая мозжечковая дегенерациярус. // Российский неврологический журнал. — 2023. — том 28. — № 4. — С. 43-53. — DOI:10.30629/2658-7947-2023-28-4-43-53
- Шнайдер Н. А., Ёжикова В. В., Дыхно Ю. А., и др. Проблемы диагностики паранеопластической мозжечковой дегенерациирус. // Неврология, нейропсихиатрия, психосоматика. — 2014. — № 1. — С. 35-43.
- Королёва Е. С., Алифирова В. М., Рязанцева А. А., Кощавцева Ю. И. Паранеопластическая мозжечковая дегенерация у пациента с антителами anti-Yo и аденокарциномой простатырус. // Бюллетень сибирской медицины. — 2017. — том 16. — № 3. — С. 218-223. — DOI:10.20538/1682-0363-2017-3-218-223
Шаблон:Паранеопластические синдромы
Одним из источников, использованных при создании данной статьи, является статья из википроекта «Рувики» («ruwiki.ru») под названием «Паранеопластическая мозжечковая дегенерация», расположенная по адресу:
Материал указанной статьи полностью или частично использован в Циклопедии по лицензии CC-BY-SA 4.0 и более поздних версий. Всем участникам Рувики предлагается прочитать материал «Почему Циклопедия?». |