Аллотропия неметаллов
Аллотропи́я немета́ллов. Аллотропией называется способность атомов одного и того же химического элемента существовать в виде нескольких простых веществ[1].
Аллотропия кислорода[править]
Кислород[править]
При нормальных условиях бесцветный газ, не имеет вкуса и запаха. Слабо растворим в воде и спирте. В жидком состоянии представляет собой бледно-голубую жидкость, в твёрдом кристаллическое вещество синего цвета. Парамагнитен. Является сильным окислителем, образует оксиды. Реагирует с водородом, при нагревании — с серой, углеродом, фософором, металлами и др.
В промышленности получают сжижением, фракционной перегонкой воздуха или электролизом воды.
Озон[править]
При нормальных условиях газ голубого цвета с резким специфическим запахом. В твёрдом виде представляет собой тёмно-синие кристаллы. Диамагнитен. Хорошо растворим в воде, в жидком состоянии смешивается во всех отношениях с жидким аргоном, азотом, метаном, фтором. Молекула озона неустойчива. Разлагается с образованием кислорода и выделением теплоты. Является сильным окислителем, образует озониды. Реагирует с алканами, их галогенпроизводными, аммиаком, углеродом, водородом и сероводородом.
Токсичен. Вызывает раздражение глаз и дыхательных путей.
В природе встречается в озоновом слое. В промышленности получают с помощью озонаторов или облучением кислорода УФ-излучением.
Аллотропия углерода[править]
Алмаз[править]
Бесцветное твёрдое вещество. Каждый атом углерода образует четыре ковалентные связи с другими атомами. При нормальных условиях метастабилен. Является самым твёрдым минералом по шкале Мооса.
Графит[править]
Слоистое вещество серо-чёрного цвета с металлическим блеском. Атомы углерода образуют шестиугольники, расположенные слоями и соединенные друг с другом ковалентными связями.
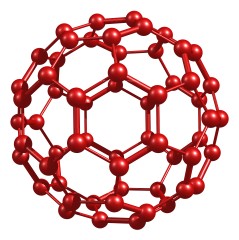
Фуллерен[править]
Замкнутые молекулы, состоящие из пятиугольников и шестиугольников с атомами углерода в вершинах. Наиболее распространённым является C60[2].
Аллотропия серы[править]
Ромбическая модификация[править]
Является наиболее устойчивой и распространённой формой при нормальных условиях. Сера (S8) в этой модификации представляет собой жёлтые кристаллы. Стабильна при температуре ниже 95,6 °C и далее переходит в моноклинную. Атомы серы в молекуле соединены ковалентными связями.
Моноклинная модификация[править]
Молекулы серы упакованы в моноклинную кристаллическую решётку. Представляет собой тёмно-жёлтые или коричневатые кристаллы. Стабильна от 95,6 до 119 С. При медленном охлаждении преобразуется в ромбическую серу[3].
Аллотропия фосфора[править]
Белый фосфор[править]
Является самой реакционноспособной модификацией фосфора. При нормальных условиях — белое или желтоватое вещество, которое легко режется ножом. При комнатной температура окисляется кислородом воздуха и происходит выделение энергии (свечение). Ядовит. Вызывает тяжёлые поражения органов, костной и нервной систем человека[4][5].
Красный фосфор[править]
Представляет собой менее реакционноспособную, но более стабильную аллотропную модификацию фосфора. На воздухе не самовоспламеняется. Нерастворим в воде, бензоле, сероуглероде и др.
Примечания[править]
- ↑ Угай Я. А. Общая и неорганическая химия: Учеб. для студентов вузов, обучающихся по направлению и спец. «Химия». — М.: Высш. шк., 1997. — 524 с.: ил.
- ↑ Молекулярное моделирование структуры фуллерена C60. Проверено 1 октября 2025.
- ↑ Эддисон У. Аллотропия химических элементов. — М.: Мир, 1966. — 207 с.
- ↑ Ходаков Ю. В., Эпштейн Д. А., Глориозов П. А. § 30. Фосфор // Неорганическая химия. Учебник для 9 класса. — 7-е изд. — М.: Просвещение, 1976. — С. 62—65. — 2 350 000 экз.
- ↑ Kemal T. Saracoglu, Ahmet H. Acar, Tamer Kuzucuoglu, Sezer Yakupoglu White phosphorus burnангл. // The Lancet. — 2010. — том 376. — № 9734. — С. 68. — DOI:10.1016/S0140-6736(10)60812-4
Одним из источников, использованных при создании данной статьи, является статья из википроекта «Рувики» («ruwiki.ru») под названием «Аллотропия неметаллов», расположенная по адресу:
Материал указанной статьи полностью или частично использован в Циклопедии по лицензии CC-BY-SA 4.0 и более поздних версий. Всем участникам Рувики предлагается прочитать материал «Почему Циклопедия?». |