Лимфома маргинальной зоны селезенки
Лимфо́ма маргина́льной зо́ны селезё́нки (ЛМЗС) — это редкая индолентная В-клеточная опухоль, поражающая селезёнку, костный мозг и кровь, которая клинически часто проявляется бессимптомным увеличением селезёнки, общей слабостью, ночной потливостью, а у примерно 20% пациентов сопровождается аутоиммунными осложнениями, такими как аутоиммунная гемолитическая анемия или иммунная тромбоцитопения. Прогноз заболевания в целом благоприятный, однако, у около 30% пациентов наблюдается трансформация в агрессивную диффузную В-крупноклеточную лимфому[1].
История[править]
Термин "спленическая маргинальная зонная лимфома" был впервые введён Шмидом и его коллегами в 1992 году, которые использовали его для описания четырёх случаев первичных В-клеточных лимфом селезёнки низкой степени злокачественности, обладавших особыми клиническими, морфологическими и иммунофенотипическими характеристиками[2].
Классификация[править]
ЛМЗС входит в общую структуру лимфом маргинальной зоны[3].
Этиология[править]
Согласно имеющимся научным данным, ведущей причиной развития ЛМЗС считается хроническая антигенная стимуляция иммунной системы. Этот процесс может быть спровоцирован персистирующими инфекциями или аутоиммунными заболеваниями. Установлена ассоциация между вирусом гепатита С и развитием ЛМЗС[3].
Патогенез[править]
Хроническая антигенная стимуляция является краеугольным камнем в развитии ЛМЗС. Наиболее убедительные доказательства этого связаны с инфекцией вируса гепатита С, которая имеет сильную эпидемиологическую связь с лимфомой, особенно в эндемичных регионах .Предполагаемые механизмы включают прямое связывание вирусного белка E2 с рецептором CD81 на В-клетках, что потенцирует сигнал от В-клеточного рецептора, а также хроническую продукцию цитокинов и факторов роста, которые поддерживают пролиферацию и выживание В-клеток[4].
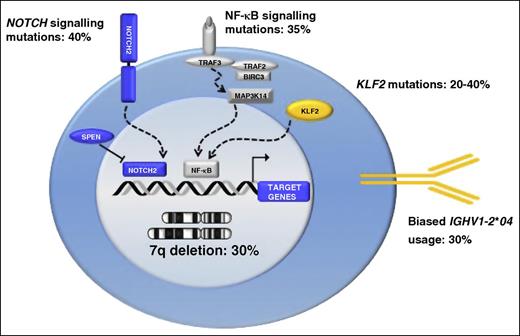
Геномные и транскриптомные исследования ЛМЗС указывают на центральную роль активации сигнального пути NF-κB в патогенезе этих заболеваний. Это подтверждается высокой распространённостью молекулярных нарушений, затрагивающих компоненты пути NF-κB, примерно у 40-50% пациентов, что делает активацию этого пути характерной чертой данных подтипов лимфом. Многочисленные исследования сообщают о сверхэкспрессии генов, вовлечённых в передачу сигнала NF-κB, включая вышестоящие сигналы от B-клеточного рецептора, Toll-подобных рецепторов и CD40, а также непосредственно NF-κB-связанных транскриптов, причём примерно у половины пациентов со СМЗЛ наблюдается ядерная экспрессия белков p50 и/или p52. Данная активация пути NF-κB является следствием совокупности геномных и эпигенетических событий. Соматические мутации в ключевых регуляторах пути, такие как мутации генов TNFAIP3, BIRC3, CARD11, MAP3K14, TRAF3 и MYD88, а также геномные повреждения KLF2, действуют согласованно с аберрантным метилированием ДНК и нарушенной экспрессией микроРНК. Следствием непрерывной передачи сигнала NF-κB является секреция провоспалительных цитокинов, таких как интрелейкин-6 и интерлейкин-2. Это создаёт петлю положительной обратной связи, которая дополнительно усиливает активацию NF-κB. Высвобождение этих цитокинов также запускает каскад киназ, которые через фосфорилирование активируют путь JAK/STAT[5].
ЛМЗС развивается в белой пульпе селезёнки, формируя бифазную гистологическую картину: средние по размеру моноцитоидные В-клетки образуют бледное кольцо вокруг фолликула по маргинальной зоне, в то время как мелкие центроцитоподобные клетки разрушают мантийную зону и колонизируют герминативные центры. Часто наблюдается плазмоцитарная дифференцировка различной степени выраженности. Неопластические клетки могут инфильтрировать красную пульпу очагово или диффузно с последующим распространением в синусы, а также часто проникают в стенки крупных сосудов. Крупные клетки встречаются редко, и их увеличение может указывать на трансформацию в более агрессивную лимфому. Инфильтрат может сопровождаться эпителиоидными гистиоцитами, иногда в таком количестве, что они маскируют опухолевые клетки. Часто вовлекаются лимфоузлы ворот селезёнки с картиной нодулярной пролиферации, облитерацией реактивных герминативных центров и инфильтрацией синусов[1].
Эпидемиология[править]
ЛМЗС представляет собой редкое заболевание, на долю которого приходится около 0.6% всех случаев неходжкинских лимфом и примерно 2% лимфоидных злокачественных новообразований, с ежегодной заболеваемостью 0.13 случая на 100 000 населения. Медиана возраста диагностирования заболевания составляет 65–70 лет, при этом эпидемиологические исследования не выявляют выраженного преобладания среди пациентов какого-либо пола[6][7].
Диагностика[править]
Клиническая картина[править]
Клиническая картина ЛМЗС характеризуется длительным и часто бессимптомным течением. Примерно у четверти пациентов на ранних стадиях заболевание не вызывает каких-либо специфических жалоб. Ключевым и основным проявлением является спленомегалия (увеличение селезёнки), которая может вызывать чувство дискомфорта, тяжести или боли в левом подреберье. По мере прогрессирования болезни присоединяются общие конституциональные симптомы: немотивированная слабость, повышенная утомляемость, снижение массы тела, ночная потливость, а иногда и кожный зуд. Несмотря на вялотекущий характер заболевания, в части случаев ЛМЗС может демонстрировать агрессивное течение с быстрым нарастанием симптоматики[3][6].
Лабораторные исследования[править]
Клинический анализ крови: возможно выявление анемии и тромбоцитопении[3].
С целью оценки общего состояния пациента и выявления сопутствующей патологии выполняются биохимический анализ крови, коагулограмма и клинический анализ мочи[3].
Иммуногистохимическое исследование биоптата селезёнки: ЛМЗС характеризуется поверхностной экспрессией IgM, CD20, CD27 и CD49d. Экспрессия других маркеров, таких как IgD, CD5, CD11c и CD25, может быть вариабельной и непостоянной. Ключевое диагностическое значение имеет отсутствие экспрессии CD103, CD123, аннексина A1 и циклина D1, что позволяет надёжно дифференцировать ЛМЗС от других В-клеточных лимфом, в частности от волосатоклеточного лейкоза и мантийноклеточной лимфомы[7].
Цитогенетический анализ крови: типичными для ЛМЗС являются делеция длинного плеча хромосомы 7 в локусе 7q22-q32 и увеличение числа копий хромосомы 3 или её длинного плеча (3q), которые встречаются примерно в четверти случаев. Часто также наблюдаются сложные перестройки, затрагивающие хромосомы 1, 3, 7, 8 и 14. Особое клиническое значение имеют делеции локуса 17p, приводящие к потере гена-супрессора опухолевого роста TP53; такие нарушения обнаруживаются у 8–20% пациентов и являются прогностически неблагоприятным фактором, ассоциированным с агрессивным течением заболевания[7].
Молекулярно-генетический анализ крови методом полногеномного секвенирования: ЛМЗС характеризуется рекуррентными мутациями в ключевых генах, регулирующих важнейшие функции В-клеток. Наиболее часто мутации генов KLF2, NOTCH2 и TP53. Также часто встречаются мутации в генах TNFAIP3, KMT2D и MYD88[7].
Инструментальные исследования[править]
Компьютерная томография и позитронно-эмиссионная томография являются методами, позволяющими стадировать заболевание и выявить опухолевые очаги вне селезёнки. Также методы используются для контроля за динамикой опухолевого процесса в процессе терапии[3].
Ультразвуковое исследование: является методом, позволяющим выявить наличие поражённых лимфатических узлов[3].
Дифференциальная диагностика[править]
Дифференциальная диагностика ЛМЗС проводится со следующими заболеваниями[1]:
- реактивная фолликулярная гиперплазия;
- хронический лимфолейкоз;
- мантийноклеточная лимфома;
- фолликулярная лимфома;
- волосатоклеточный лейкоз;
- диффузная В-клеточная лимфома селезёночной красной пульпы;
- лимфоплазмоцитарная лимфома;
- вторичное поражение селезёнки при экстранодальной лимфоме маргинальной зоны;
- нодальная лимфома маргинальной зоны;
- моноклональный В-клеточный лимфоцитоз.
Осложнения[править]
При ЛМЗС возможно развитие аутоиммунными осложнений, например, аутоиммунной гемолитической анемии или иммунной тромбоцитопении[1].
Основные осложнения при ЛМЗС связаны со спленэктомией. Их можно разделить на непосредственные и отдалённые[1]:
- к непосредственным осложнениям спленэктомии относятся: нарушение функции лёгких, развитие тромбоза глубоких вен или тромбоза воротной вены, а также кровотечения;
- главным отдалённым осложнением является повышенная восприимчивость к бактериальным инфекциям.
Лечение[править]
Лечение ЛМЗС начинается при наличии определённых показаний, к которым относятся симптоматическая и прогрессирующая спленомегалия, значительная цитопения (снижение количества эритроцитов, тромбоцитов или нейтрофилов) и развитие аутоиммунных осложнений. При отсутствии этих явлений допустима тактика динамического наблюдения[3].
Стратегия лечения зависит от инфицирования пациента вирусом гепатита С. При его выявлении первоочередной мерой является проведение противовирусной терапии, что часто приводит к регрессу лимфомы. Пациентам без данной инфекции или при невозможности противовирусного лечения предлагаются следующие варианты: монотерапия ритуксимабом, иммунохимиотерапия или спленэктомия[3].
Спленэктомия рассматривается при значительном увеличении селезёнки, угрозе её разрыва, выраженной цитопении или при противопоказаниях к лекарственной терапии. Удаление селезёнки быстро улучшает показатели крови и устраняет симптомы, оно не приводит к полной ремиссии, так как опухолевые клетки остаются в костном мозге и лимфоузлах. Обязательной мерой при планировании операции является вакцинация против пневмококка, менингококка и гемофильной палочки[3].
Прогноз[править]
ЛМЗС характеризуется благоприятным прогнозом. При отсутствии выраженного гиперспленизма и признаков прогрессирования заболевания медиана выживаемости пациентов может превышать 10 лет[6].
Диспансерное наблюдение[править]
Взрослым пациентам, завершившим лечение по поводу ЛМЗС с достижением полной ремиссии, рекомендуется регулярное диспансерное наблюдение у врача-онколога или врача-гематолога. График наблюдения предполагает осмотры каждые 3 месяца в течение первого года после завершения терапии, каждые 6 месяцев в течение второго года, а затем ежегодно. После пяти лет, при условии достижения стойкой ремиссии, осмотры могут проводиться раз в два года. Программа диспансерного наблюдения включает тщательный сбор жалоб, клинический осмотр пациента, рентгенографию органов грудной клетки, ультразвуковое исследование брюшной полости и периферических лимфатических узлов[3].
Профилактика[править]
Не разработана[3].
Примечания[править]
- ↑ 1,0 1,1 1,2 1,3 1,4 Arcaini L., Rossi D., Paulli M. Splenic marginal zone lymphoma: from genetics to managementангл. // Blood. — 2016. — том 127. — № 17. — С. 2072-2081. — DOI:10.1182/blood-2015-11-624312
- ↑ Mishra N.M., Pandey R., Dinda A., Nityanand S. A Peculiar Case of Splenic Marginal Zone Lymphoma and Review of Literatureангл. // Iran J Immunol. — 2013. — том 10. — № 3. — С. 186-189. — DOI:10.22034/iji.2013.16835
- ↑ 3,00 3,01 3,02 3,03 3,04 3,05 3,06 3,07 3,08 3,09 3,10 3,11 Российское общество онкогематологов, Национальное гематологическое общество, Ассоциация онкологов России Лимфома маргинальной зонырусский. Министерство Здравоохранения Российской Федерации (20.12.2023). Проверено 6 ноября 2025.
- ↑ Du M.-Q. Pathogenesis of splenic marginal zone lymphomaангл. // Pathogenesis. — 2015. — том 2. — № 4. — С. 11-20. — ISSN 2214-6636. — DOI:10.1016/j.pathog.2015.07.001
- ↑ Spina V., Mensah A.A., Arribas A.J. Biology of splenic and nodal marginal zone lymphomasангл. // Annals of Lymphoma. — 2021. — том 5. — ISSN 2616-2695.
- ↑ 6,0 6,1 6,2 Zhang S., Xuan Z., Zhang L. et al. Splenic marginal zone lymphoma: a case report and literature reviewангл. // World J Surg Onc. — 2020. — том 18. — С. 259. — DOI:10.1186/s12957-020-02030-3
- ↑ 7,0 7,1 7,2 7,3 Mirandari A., Parker H., Ashton-Key M. et al. The genomic and molecular landscape of splenic marginal zone lymphoma, biological and clinical implicationsангл. // Explor Target Antitumor Ther. — 2024. — том 5. — № 4. — С. 877-901. — DOI:10.37349/etat.2024.00253
Литература[править]
- Хвастунова А.Н., Аль-Ради Л.С., Федянина О.С., Джулакян У.Л., Капранов Н.М., Закирова А.О., Луговская С.А., Наумова Е.В., Атауллаханов Ф.И., Кузнецова С.А. Особенности морфологии и иммунофенотипа опухолевых клеток лимфомы из клеток маргинальной зоны селезёнки (исследование с помощью клеточного биочипа)рус. // Онкогематология. — 2017. — том 12. — № 1. — С. 71-77. — DOI:10.17650/1818-8346-2017-12-1-71-77
- Arcaini L., Rossi D., Paulli M. Splenic marginal zone lymphoma: from genetics to managementангл. // Blood. — 2016. — том 127. — № 17. — С. 2072-2081. — DOI:10.1182/blood-2015-11-624312
- Zhang S., Xuan Z., Zhang L. et al. Splenic marginal zone lymphoma: a case report and literature reviewангл. // World J Surg Onc. — 2020. — том 18. — С. 259. — DOI:10.1186/s12957-020-02030-3
- Mirandari A., Parker H., Ashton-Key M., Stevens B., Walewska R., Stamatopoulos K., Bryant D., Oscier D.G., Gibson J., Strefford J.C. The genomic and molecular landscape of splenic marginal zone lymphoma, biological and clinical implicationsангл. // Explor Target Antitumor Ther. — 2024. — том 5. — № 4. — С. 877-901. — DOI:10.37349/etat.2024.00253
- Российское общество онкогематологов, Национальное гематологическое общество, Ассоциация онкологов России. Лимфома маргинальной зоны (рус.). Рубрикатор клинических рекомендаций. Министерство Здравоохранения Российской Федерации (20 декабря 2023). Дата обращения: 6 ноября 2025.
Шаблон:Лимфоидное злокачественное новообразование
Одним из источников, использованных при создании данной статьи, является статья из википроекта «Рувики» («ruwiki.ru») под названием «Лимфома маргинальной зоны селезенки», расположенная по адресу:
Материал указанной статьи полностью или частично использован в Циклопедии по лицензии CC-BY-SA 4.0 и более поздних версий. Всем участникам Рувики предлагается прочитать материал «Почему Циклопедия?». |