Родопсин
→ Опсины
Родопси́н (от др.-греч. ρόδον — роза и др.-греч. όπσις — зрение; иногда в качестве синонима используют устаревшее название — зри́тельный пу́рпур) — группа зрительных пигментов, несколько различных по строению у разных видов животных (см. опсины). Содержится в палочках сетчатки глаза морских беспозвоночных, рыб, почти всех наземных позвоночных и человека. Относится к сложным белкам — хромопротеинам.
Модификации белка, свойственные различным биологическим видам, могут существенно различаться по структуре и молекулярной массе.
Родопсин принадлежит к обширному семейству G-белоксопряжённых рецепторов (GPCR-рецепторов), названному так за механизм трансмембранной передачи сигнала, основанный на взаимодействии с внутриклеточными примембранными G-белками. Появление его пространственной структуры, полученной с высоким экспериментальным разрешением, является очень важным событием для биологии и медицины, поскольку родопсин как «родоначальник» семейства А GPCR-рецепторов является своего рода «моделью» структуры и функций множества других рецепторов, чрезвычайно интересных с фундаментальной и практической (фармакологической) точек зрения. Свое название родопсин получил за ярко-красный цвет (по-гречески rhodon — означает «розовый», a opsis — зрение).
История открытия и исследований родопсина[править]
Пурпурная окраска клеток-палочек была обнаружена Генрихом Мюллером (Heinrich Müller) в 1851 году; он приписал её гемоглобину. Он извлек из глаза лягушки сетчатку; она оказалась розовато-пурпурной, но очень скоро обесцветилась. Это столь интересное наблюдение было забыто.
В 1876 году Франц Болл (Franz Boll, 1876) из Римского университета выделил фоточувствительный пигмент из палочки сетчатки лягушки. Он обнаружил, что сетчатка лягушки чувствительна к свету, и после освещения меняет свою окраску на жёлтую, с последующим обесцвечиванием. Болл также продемонстрировал, что после некоторого времени пребывания в темноте сетчатка животных приобретает изначальную яркую окраску.
Вилли Кюхне (Willy Kühne), физиолог из Германии, продолживший работы Франца Болла, определил, что пигмент, отвечающий за окраску сетчатки — это белок наружных сегментов палочек (НСП), и назвал его «зрительным пурпуром» (родопсином). Кюхне выделил родопсин из клеток пигментного эпителия сетчатки, сравнил спектроскопические свойства этого белка и препарата сетчатки. Он постулировал, что жёлтый и бесцветный продукты, образующиеся под действием света, химически различны, и заключил, что генерация сетчаткой электрических импульсов является следствием реакции на свет.
В 1933 году строение и химические свойства родопсина были изучены Джорджем Уолдом и его коллегами по Гарвардскому университету, которые впервые выделили из препарата сетчатки вещество, первоначально идентифицированное как витамин А, что объяснило феномен «куриной слепоты» у пациентов с авитаминозом по этому каротиноиду (к тому времени еще мало было известно о биохимической роли витаминов). Позже оказалось, что кофактором является ретиналь — соответствующий витамину А (ацетату ретинола) альдегид. Уолд и коллеги продемонстрировали, что ретиналь, добавленный в темноте к обесцвеченному родопсину, способен восстанавливать «свежий» пигмент, причём этим действием обладает только 11-цис-изомер. Они открыли, что родопсин состоит из двух компонентов — бесцветного белка, называемого опсином или жёлтым пигментом и 11-цис-ретиналя, ковалентно связанного хромофора каротиноидной природы, акцептирующего свет. В 1967 году Уолд получил Нобелевскую премию по физиологии и медицине «за исследования в области физиологии и биохимии зрения», а также за открытие биохимической роли витамина А (см. Нобелевская речь Уолда, 1967, на англ. языке).
Полная аминокислотная последовательность родопсина была определена в 1982 году в Институте биоорганической химии АН СССР Ю. А. Овчинниковым и сотр. и несколько позже подтверждена анализом структурного гена родопсина Д. Хоггнесом и Дж. Натансом в США. Было показано, что в последовательности родопсина длиной 348 аминокислотных остатков присутствует семь протяжённых участков, состоящих из неполярных аминокислотных остатков, образующих трансмембранные (ТМ) α-спирали, соединенные вне- и внутриклеточными участками-«петлями». При этом N-конец находится во внеклеточной области, а C-конец — в цитоплазматической. Такая топология рецептора была подтверждена ограниченным протеолизом белка в составе нативной мембраны, обработкой моноклональными антителами и химической модификацией проникающими и непроникающими агентами. Также было установлено место прикрепления кофактора: ретиналь связывается альдиминной связью с остатком ЛИЗ-296, находящимся в седьмой (последней) ТМ α-спирали.
Пространственная структура родопсина долго не поддавалась изучению «прямыми» методами, рентгеноструктурным анализом (РСА) и спектроскопией ядерного магнитного резонанса (ЯМР). В то время как атомная структура другого мембранного белка, со схожей семиспиральной топологией (бактериородопсин) была определена Гендерсоном и сотр. еще в 1990-м году, структура зрительного родопсина высокого разрешения оставалась неизвестной до 2000 года.
Структура молекулы родопсинов[править]
Родопсины микроорганизмов[править]
Родопсины млекопитающих[править]
Функции родопсина[править]
Под действием света светочувствительный зрительный пигмент изменяется и один из промежуточных продуктов его превращения непосредственно ответствен за возникновение зрительного возбуждения. Зрительные пигменты, содержащиеся в наружном сегменте фоторецепторной клетки, представляют собой сложные окрашенные белки (хромопротеиды). Та их часть, которая поглощает видимый свет, называется хромофором. Это химическое соединение — альдегид витамина А, или ретиналь. Белок зрительных пигментов, с которыми связан ретиналь, называется опсином.
При поглощении кванта света (фотона) хромофорная группа белка (11-цис-ретиналь) изомеризуется в транс-форму. Возбуждение зрительного нерва происходит при фотолитическом разложении родопсина за счёт изменения ионного транспорта в фоторецепторе. Впоследствии родопсин восстанавливается (регенерирует) в результате синтеза 11-цис-ретиналя и опсина или в процессе синтеза новых дисков наружного слоя сетчатки.
Родопсин относится к суперсемейству трансмембранных рецепторов GPCR (рецепторов, связанных с G-белками). При поглощении света конформация белковой части родопсина меняется, и он активирует G-белок трансдуцин, который активирует фермент цГМФ-фосфодиэстеразу. В результате активации этого фермента в клетке падает концентрация цГМФ и закрываются цГМФ-зависимые натриевые каналы. Так как ионы натрия постоянно выкачиваются из клетки АТФ-азой, концентрация ионов натрия внутри клетки падает, что вызывает её гиперполяризацию. В результате фоторецептор выделяет меньше тормозного медиатора глутамата, и в биполярной нервной клетке, которая «растормаживается», возникают нервные импульсы.
Спектр поглощения родопсина[править]
Специфический спектр поглощения зрительного пигмента определяется как свойствами хромофора и опсина, так и характером химической связи между ними (подробнее об этом см. обзор:[1]). Этот спектр имеет два явных максимума — один в ультрафиолетовой области (278 нм.), обусловленный опсином, и другой — в видимой области (около 500 нм.), — поглощение хромофора рис. 1. Превращение при действии света зрительного пигмента до конечного стабильного продукта состоит из ряда очень быстрых промежуточных стадий. Исследуя спектры поглощения промежуточных продуктов в экстрактах родопсина при низких температурах, при которых эти продукты стабильны, удалось подробно описать весь процесс обесцвечивания зрительного пигмента[2].
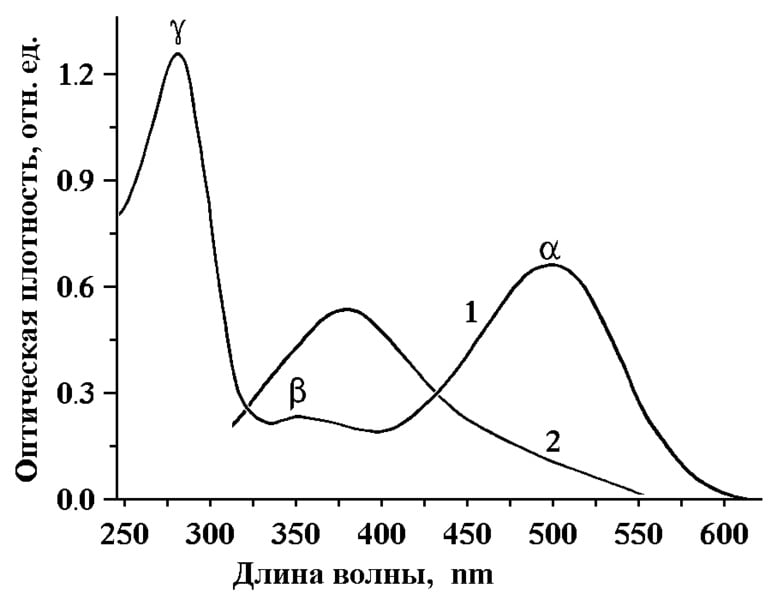
На Рис. 1 показаны спектры поглощения родопсина лягушки Rana temporaria в дигитониновом экстракте. По оси абсцисс — длина волны (λ); по оси ординат — оптическая плотность (D).
На спектре поглощения восстановленного родопсина (измеренного при слабом освещении, график 1) видны два основных максимума поглощения в видимой (500 нм.) и ультрафиолетовой (280 нм.) области. На спектре поглощения обесцвеченного родопсина (измеренного при сильном освещении, график 2) наблюдается единственный максимум поглощения с длиной волны 380 нм.
Спектр поглощения родопсина, содержит три основные полосы: α — (500 нм), β — (350 нм), γ — (280 нм). Полосы α — (500 нм) и β — (350 нм) относятся к области поглощения хромоформной группы. Полоса γ — (280 нм) — относится к группе поглощения ароматических аминокислот белка — триптофана, тирозина и фенилаланина. Так α-полоса в спектре поглощения родопсина расположена на графике кривой палочкового сумеречного видения (зрения) с предельной величиной в зоне лучей сине-зелёной области спектра (то есть 500нм).[3]
В хрусталике глаза и тканях сетчатки существует пигмент типа меланина, анологичный тому, что содержится в коже. Он имеет желтоватый или коричневый оттенок и служит для того, чтобы предотвратить попадание определённой части световой энергии, в особенности коротковолновой энергии, на сетчатку. При этом он является светофильтром отсекающим губительную для тканей и рецепторов УФ область спектра[4].[5]. Поэтому, при достаточном для различения цветов уровне освещения, максимум чувствительности палочки (в которой содержится родопсин) находится не в ультрафиолетовой, а в синей части спектра.
В живом глазу наряду с разложением зрительного пигмента, естественно, постоянно идёт процесс его регенерации (ресинтеза). При темновой адаптации этот процесс заканчивается только тогда, когда весь свободный опсин соединился с ретиналем.[6]
Дневное и ночное зрение[править]
Из спектров поглощения родопсина видно, что восстановленный родопсин (при слабом «сумеречном» освещении) отвечает за ночное зрение, а при дневном «цветовом зрении» (ярком освещении) разлагается, его фоточувствительность уменьшается, а максимум его чувствительности смещается в синюю область. Это наглядно показывает известный Эффект Пуркинье.[7].
С родопсином связан также эффект Пуркинье, который вызван более высокой чувствительностью колбочек в сетчатке глаза к желтому свету, тогда как палочки более чувствительны к синему свету, но при этом только палочки неспособны обеспечить цветное зрение. В результате красные цвета в сумерках кажутся более тёмными, нежели зелёные, а в ночное время — практически чёрными, в то время как синие объекты «становятся» более светлыми. В условиях низкой освещённости, когда колбочкам недостаточно света для функционирования, человек «видит» палочками, но в чёрно-белом цвете.
Полное восстановление родопсина у человека (в темноте или при слабом освещении) занимает около 30 минут; в течении всего этого периода чувствительность «сумеречного зрения» человека постепенно увеличивается, достигая максимума.
См. также[править]
Источники[править]
- ↑ Островский М. А., Федорович С. Е., Голубев И. Н., 1967, Биофизика, 12 : 877.
- ↑ Hubbard R., Bownds D., Yoshizawa T., 1965. Cold Spring Harbor Symp. Biol., 30 : 301.
- ↑ http://library.biophys.msu.ru/PDF/3353.pdf
- ↑ Deane B. Judd and Gunter Wyszecki, Color in business, science and industry, New York/London/Sydney/Toronto, 1975.
- ↑ Д. Джадд, Г. Вышецки, Цвет в науке и технике, Изд. «мир», Москва 1978 г., стр 25.
- ↑ АН СССР, объединённый научный совет «физиология человека и животных», Физиология сенсорных систем. Ч. 1. Физиология зрения. 1971 г., Издательство «Наука», Ленинградское отделение. Стр. 94 — 101
- ↑ Ричард Филлипс Фейнман. Фейнмановские Лекции по Физике, том № 3, гл. 35 (Цветовое зрение), стр. 157.
Литература[править]
- Страйер Л., Биохимия. пер. с англ., т. 3, М., 1985, с. 340—348
- Абдулаев, Нажмутин Гаджимагомедович. Родопсины: структура и функции. Автореф. д.х.н., М., 1985
- N. N. Vsevolodov. Biomolecular electronics: an introduction via photosensitive proteins
- Ovchinnikov Yu. А., «FEES letters», 1982, v. 148(2), p. 179—191
- Applebury M., Hargrave P., «Visual Res.», 1986, v. 26 (12), p. 1881—1895
- Shichida Y., «Photobio-chemistry and Photobiophysics», 1986, v. 13 (3), p. 287—307
- Pugh E., Cobbs W., «Visual Res.», 1986, v. 26 (10), p. 1613—1643
- Bennett N.. Sitaramayya A., «Biochemistry», 1988, v. 27 (5), p. 1710—1715
Ссылки[править]
- The Rhodopsin Protein
- Photoisomerization of rhodopsin, animation.
- Rhodopsin and the eye, summary with pictures.