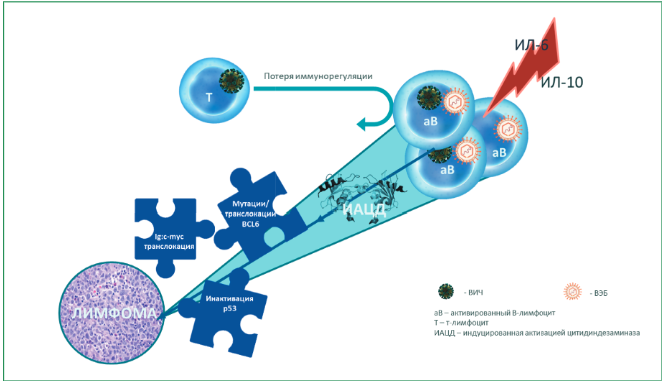
СПИД-ассоциированная лимфома
СПИД-ассоциированные лимфомы — это группа злокачественных лимфопролиферативных заболеваний, развивающихся на фоне иммунодефицита, вызванного вирусом иммунодефицита человека. Ключевым патогенетическим фактором является угнетение противоопухолевого иммунитета, что приводит к значительному повышению риска возникновения лимфом. Наиболее распространёнными формами являются диффузная крупноклеточная В-клеточная лимфома, лимфома Беркитта. Несмотря на снижение частоты этих лимфом в эру антиретровирусной терапии, они остаются одной из ведущих причин смертности у ВИЧ-инфицированных, особенно при низком уровне CD4+ лимфоцитов и агрессивных гистологических вариантах опухоли[1][2].
История[править]
Связь между вирусом иммунодефицита человека и лимфомой была выявлена на ранних этапах эпидемии синдрома приобретённого иммунодефицита (СПИД). Уже в 1982 году, вскоре после первых сообщений о синдроме, были зарегистрированы случаи агрессивной лимфомы, сходной с лимфомой Беркитта, у инфицированных лиц. Последующие исследования подтвердили, что ВИЧ-инфекция существенно повышает риск развития определённых типов лимфом. Эти ВИЧ-ассоциированные лимфомы, (лимфома Беркитта, диффузная В-крупноклеточная лимфома и первичная лимфома центральной нервной системы) были официально включены в перечень СПИД-индикаторных заболеваний в 1987 году. Позднее, после открытия герпесвируса, ассоциированного с саркомой Капоши, в 1994 году, были описаны и другие специфические нозологические формы, такие как первичная выпотная лимфома и плазмобластная лимфома[3].
Классификация[править]
Классификация лимфоидных новообразований, ассоциированных с ВИЧ, Всемирной организации здравоохранения от 2016 года включает следующие нозологии[1]:
- диффузная крупноклеточная В-клеточная лимфома:
- центробластная;
- иммунобластная (включая первичную лимфому центральной нервной системы);
- лимфома Беркитта
- экстранодальная MALT-лимфома;
- периферическая Т-клеточная лимфома;
- лимфомы, более специфичные для ВИЧ-инфицированных пациентов:
- первичная выпотная лимфома;
- плазмобластная лимфома ротовой полости;
- лимфомы, встречающиеся при других иммунодефицитных состояниях
Этиология[править]
Этиологией развития данного типа лимфом является СПИД на фоне ВИЧ-инфекции. Основными типами опухолей в данной категории пациентов являются диффузная крупноклеточная В-клеточная лимфома, первичная лимфома центральной нервной системы, лимфома Беркитта, первичная выпотная лимфома, плазмобластная лимфома и лимфома Ходжкина, которые характеризуются агрессивным течением[2].
Патогенез[править]
Развитие СПИД-ассоциированных лимфом обусловлено комбинированным действием прямых и непрямых механизмов. Прямое онкогенное воздействие осуществляется через вирусные белки, которые проникают в В-лимфоциты и запускают злокачественную трансформацию. Матричный белок p17, способный самостоятельно индуцировать развитие лимфомы, накапливается в лимфоидной ткани и активирует сигнальный путь PAR1/EGFR/PI3K/Akt. Белок Tat усиливает экспрессию онкогена MYC, провоцирует хромосомные аберрации и способствует онкогенным перестройкам MYC-IGH. Оба белка индуцируют аномальную активность цитидиндезаминазы, повышая геномную нестабильность В-клеток. Хотя Т-клеточные лимфомы встречаются реже, хроническая ВИЧ-инфекция способствует злокачественной трансформации Т-лимфоцитов через интеграцию провируса в гены STAT3 и LCK, а также индукцию анеуплоидии. Также важную роль играют иммуносупрессия, нарушающая функцию естественных киллеров, Т-клеток и макрофагов, и коинфекция онкогенными вирусами[4].
Косвенный механизм канцерогенеза при ВИЧ-ассоциированных лимфомах реализуется через комплексное нарушение иммунной регуляции и хроническое воспаление. Иммуносупрессия проявляется дисфункцией ключевых иммунных популяций. Одновременно наблюдается подавление цитотоксической активности NK-клеток через снижение экспрессии NKG2D и азтосодержащих радикалов, а также истощение CD4+ лимфоцитов в сочетании с гиперэкспрессией ингибиторных рецепторов PD-1 и SOCS-7 на CD8+ T-клетках. На уровне В-клеток отмечается стойкое повышение экспрессии белка BAFF, ведущее к нарушению дифференцировки маргинальной зоны и снижению функции B-регуляторных клеток. Дополнительным фактором выступает коинфекция онкогенными вирусами, где вирус Эпштейна — Барр и Т-лимфотропный вирус человека-1 синергично усиливают лимфопролиферацию через механизмы клональной экспансии. Совокупность хронического воспаления, иммунной дисрегуляции и вирусной коинфекции создаёт условия для ускользания опухолевых клеток от иммунного надзора и прогрессии лимфом[4].
Важную роль в патогенезе при СПИД-ассоциированных лимфомах играет опухолевая иммунная микросреда, которая представляет собой динамическую систему взаимодействия между опухолевыми клетками, иммунными клетками и внеклеточным матриксом. В её состав входят опухолеассоциированные макрофаги, NK-клетки, Т- и В-лимфоциты, онкогенные вирусы и цитокины, которые совместно участвуют в патогенезе заболевания. Согласно имеющимся в научной литературе данным, иммунные клетки изначально выполняют противоопухолевую функцию на ранних стадиях опухолевого развития, однако по мере прогрессирования заболевания постепенно приобретают онкогенный фенотип. Этот переход способствует формированию иммуносупрессии, обеспечивает ускользание опухоли от иммунного надзора и стимулирует отдалённое метастазирование[4].
Эпидемиология[править]
Эпидемиологические исследования демонстрируют значительную эволюцию структуры СПИД-ассоциированных лимфом на фоне широкого внедрения комбинированной антиретровирусной терапии. Согласно данным Швейцарской когорты, пик заболеваемости неходжкинскими лимфомами пришёлся на 1993-1995 годы с показателем 13,6 случаев на 1000 человеко-лет, тогда как к 2002-2006 годам этот показатель снизился до 1,8. Индийское ретроспективное исследование выявило, что на СПИД-ассоциированные лимфомы приходится 6,5% всех случаев лимфом, с преобладанием диффузной крупноклеточной В-клеточной лимфомы (47,1%), плазмобластной лимфомы (21,4%) и лимфомы Ходжкина (17,1%). Данных по распространённости на территории Российской Федерации нет[5].
Диагностика[править]
Клиническая картина[править]
Клиническая картина во многом определяется конкретной гистологической формой лимфомы. СПИД-ассоциированные лимфомы характеризуются агрессивным течением с преобладанием экстранодального поражения. Типичной особенностью является множественное вовлечение органов, включая желудочно-кишечный тракт, центральную нервную систему, печень, костный мозг, органы ротовой полости, сердце и перикард, лёгкие, кожные покровы, яички и молочные железы. Периферические лимфатические узлы поражаются лишь у трети пациентов. Клиническая картина обычно проявляется поздней стадией ВИЧ-инфекции с характерными системными проявлениями: лихорадкой, значительной потерей массы тела и массивными опухолевыми очагами. Особенностью течения является частое сочетание лимфомы с другими оппортунистическими инфекциями, среди которых ведущее место занимает туберкулёз, а также бактериальные, вирусные и грибковые инфекции[6][7].
Лабораторные исследования[править]
Гистологическое исследование биоптата:
- лимфома Беркитта: опухолевые клетки характеризуются округлыми ядрами с ажурным хроматином и могут содержать несколько мелких ядрышек. Цитоплазма клеток обладает выраженной базофилией и содержит заметные вакуоли. При окраске гематоксилином и эозином наблюдаются чёткие цитоплазматические границы, создающие эффект "спрессованности" клеток. Среди морфологических вариантов выделяют плазмоцитоидный и плеоморфный типы. Для опухоли характерна высокая пролиферативная активность с большим количеством митотических фигур, что сочетается с интенсивным апоптозом. В гистологических препаратах это проявляется классической картиной "звёздного неба", образуемой макрофагами, содержащими клеточный детрит[8].
- лимфома Ходжкина: нодулярный вариант характеризуется частично нодулярным ростом с фиброзными тяжами и преобладанием лакунарных клеток. Смешанноклеточный вариант демонстрирует диффузный или слабо нодулярный рост без фиброзных тяжей с выраженным воспалительным фоном и типичными клетками Рид — Штернберга. Вариант с лимфоцитарным преоблданаием отличается нодулярным ростом с преимущественно лимфоцитарным инфильтратом при минимальном количестве эозинофилов и нейтрофилов[9].
- первичная выпотная лимфома: опухолевые клетки первичной выпотной лимфомы демонстрируют значительный полиморфизм в биологических жидкостях - от крупных иммунобластных и плазмобластных форм до анапластических вариантов. Клетки характеризуются крупными ядрами с округлыми или неровными контурами, выраженными ядрышками и обильной базофильной цитоплазмой. Часть клеток проявляет признаки плазмоцитоидной дифференцировки с перинуклеарным просветлением. В некоторых случаях наблюдаются многоядерные клетки, напоминающие клетки Рид — Штернберга. При экстракавитарных формах первичной выпотной лимфомы опухолевые клетки могут иметь более мономорфный вид с характерным поражением лимфатических синусов и сосудистых структур, что морфологически может имитировать анапластическую крупноклеточную лимфому или интраваскулярную лимфому[10].
- плазмобластная лимфома: опухоль характеризуется диффузным характером роста и состоит из крупных В-клеток. Морфологически клетки представлены центробластами и иммунобластами, а при экстранодальных локализациях часто демонстрируют признаки плазмоцитарной дифференцировки в виде плазмобластов и более зрелых плазмоцитоидных элементов. Характерными гистологическими особенностями являются обширные участки некроза, скопления апоптотических телец, а в части случаев - классическая картина "звёздного неба" за счёт присутствия макрофагов, содержащих клеточный детрит[11].
- первичная лимфома центральной нервной системы: типичная морфологическая картина характеризуется опухолью без чёткой структурной организации с обширными участками некрозов и вазоцентрическим типом роста, преимущественно выявляемым на периферии новообразования. Инвазивный фронт может иметь как чёткие границы, так и проявляться диффузной инфильтрацией с проникновением отдельных опухолевых клеток в окружающие ткани. Опухолевые клетки отличаются крупными размерами и полиморфизмом, содержат округлые или овальные везикулярные ядра с хроматином и выраженными ядрышками, при скудной цитоплазме, что морфологически сходно с центробластами или иммунобластами. Характерными признаками являются высокая митотическая активность и частое наличие апоптотических телец[12].
- диффузная крупноклеточная В-клеточная лимфома: характеризуется сочетанием малых и крупных клеток в приблизительно равных пропорциях. Малые клетки обычно превосходят по размерам нормальные лимфоциты, имеют расщеплённые или вдавленные ядра с грубым распределением хроматина. Крупные клетки представлены как клетками с расщеплёнными ядрами, так и нерасщеплёнными вариантами. Цитоплазма этих клеток отличается бледной окраской, ядра имеют неправильную форму с центральной инвагинацией и малозаметными ядрышками. Отдельная субпопуляция крупных клеток обладает округлыми ядрами с одним или несколькими ядрышками - это нерасщеплённые крупные клетки, по размерам несколько превосходящие клетки с расщеплёнными ядрами[13].
Иммуногистохимическое исследование биоптата опухоли[2]:
- при диффузной В-крупноклеточной лимфоме центробластный вариант характеризуется экспрессией маркеров CD20, CD10 и BCL6, в то время как иммунобластный тип демонстрирует плазмоцитоидную дифференцировку с позитивностью MUM1/IRF4 и CD138 при отсутствии CD10;
- для лимфомы Беркитта патогномоничными признаками являются высокая пролиферативная активность (Ki67 >95%), экспрессия CD10 и CD20 при отсутствии BCL2;
- первичная выпотная лимфома обладает уникальным "нулевым" фенотипом с отсутствием стандартных В- и Т-клеточных маркеров при экспрессии CD45, CD30, CD38 и CD138, что свидетельствует о плазмобластической дифференцировке;
- плазмобластная лимфома характеризуется утратой В-клеточных маркеров и экспрессией плазмоцитарных антигенов, таких как CD138, CD38 и MUM1;
- первичная лимфома центральной нервной системы: обычно экспрессирует панель В-клеточных маркеров, включая CD19, CD20, CD22 и CD79a, при этом плазмоцитарные маркеры CD38 и CD138 часто отсутствуют[12].
Для оценки общего состояния пациента выполняются клинический анализ крови, коагулограмма и биохимический анализ крови[14].
Для оценки иммунного статуса у пациентов с ВИЧ-инфекцией проводится оценка иммунорегуляторного индекса, которые определяется по соотношению CD4/CD8 клеток и количественное определение РНК вируса иммунодефицита человека человека в плазме крови методом полимеразной цепной реакции (ПЦР)[14].
Дифференциальная диагностика[править]
Дифференциальная диагностика СПИД-ассоциированных лимфом проводится со следующими состояниями[15]:
- персистирующая генерализованная лимфаденопатия;
- туберкулёз;
- нетуберкулёзные микобактериозы;
- синдром восстановления иммунитета при ВИЧ;
- болезнь Кастлемана;
- синдром диффузного инфильтративного лимфоцитоза.
Лечение[править]
Современные методы лечения ВИЧ-ассоциированных лимфом включают три основных направления терапии;
- моноклональные антитела демонстрируют эффективность при различных типах лимфом: ритуксимаб (анти-CD20) в комбинации с химиотерапией улучшает выживаемость при диффузной крупноклеточной В-клеточной лимфоме; брентуксимаб ведотин (анти-CD30) показал результативность при первичной выпотной лимфоме; даратумумаб (анти-CD38) исследуется при плазмобластной лимфоме;
- ингибиторы контрольных точек, такие как пембролизумаб (анти-PD-1) и ипилимумаб (анти-CTLA-4), применяются при рецидивирующих и рефрактерных формах лимфом, демонстрируя потенциал в реактивации противоопухолевого и противовирусного иммунитета;
- клеточные методы терапии включают аллогенную трансплантацию гемопоэтических стволовых клеток и CAR-T-терапию, направленную против CD19, которая показала обнадёживающие результаты в ограниченном числе случаев. Перспективность этих подходов требует дальнейшего изучения в рамках масштабных клинических исследований для определения их оптимального места в лечении СПИД-ассоциированных лимфом[4].
Прогноз[править]
Прогноз при СПИД-ассоциированной лимфоме Ходжкина определяется рядом факторов. Неблагоприятными прогностическими маркерами являются вовлечение костного мозга и повышенное количество моноцитов в периферической крови. Дополнительным негативным фактором служит соотношение лимфоциты/моноциты ниже 1,09. Пятилетняя выживаемость в этой группе пациентов остаётся существенно ниже по сравнению с СПИД-негативными больными лимфомами[5].
Диспансерное наблюдение[править]
Наблюдение пациентов со СПИД-ассоциированными лимфомами проводится по основному заболеванию[14].
| Сроки от начала антиретровирусной терапии (АРТ) | Осмотр, консультирование | Исследования |
|---|---|---|
| Через 1 мес от начала АРТ | - Анамнез;
- Физикальный осмотр; - Консультирование по вопросам АРТ; - Оценка приверженности АРТ |
- Исследование вирусной нагрузки (ВН) ВИЧ (количественное определение РНК ВИЧ-1 в плазме крови методом ПЦР) [131];
- Клинический анализ крови; - Определение активности аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ) в крови; - Исследование концентрации креатинина в крови |
| Через 2 мес от начала АРТ | - Анамнез;
- Физикальный осмотр; - Консультирование по вопросам АРТ; - Оценка приверженности АРТ |
Исследование ВН ВИЧ (количественное определение РНК ВИЧ-1 в плазме крови методом ПЦР) (проводится в случае, если за первый месяц лечения ВН ВИЧ снизилась менее, чем в 10 раз) |
| Через 3 мес от начала АРТ | - Анамнез;
- Физикальный осмотр; - Консультирование по вопросам АРТ; - Оценка приверженности АРТ |
- Исследование ВН ВИЧ (количественное определение РНК ВИЧ-1 в плазме крови методом ПЦР), исследование CD4+ лимфоцитов;
- Клинический анализ крови; - Определение активности АЛТ, АСТ, исследование уровня креатинина в крови - Клинический анализ мочи |
| Затем каждые
3-4 месяца до снижения ВН ВИЧ ниже уровня определения и роста CD4 ≥500 кл/мкл |
- Анамнез;
- Физикальный осмотр; - Консультирование по вопросам АРТ; - Оценка приверженности АРТ |
- Исследование ВН ВИЧ (количественное определение РНК ВИЧ-1 в плазме крови методом ПЦР), исследование CD4+ лимфоцитов;
- Клинический анализ крови; - Определение активности АЛТ, АСТ в крови; - Исследование уровня креатинина в крови; - Клинический анализ мочи. |
| Далее каждые
6 месяцев (при CD4 ≥500 кл/мкл и ВН ВИЧ ниже уровня определения) |
- Анамнез;
- Физикальный осмотр; - Консультирование по вопросам АРТ; - Оценка приверженности АРТ |
- Исследование ВН ВИЧ (количественное определение РНК ВИЧ-1 в плазме крови методом ПЦР), исследование CD4+ лимфоцитов;
- Клинический анализ крови; - Определение активности АЛТ, АСТ в крови; - Исследование уровня креатинина в крови; - Клинический анализ мочи |
Профилактика[править]
Профилактика СПИД-ассоциированных лимфом сводится к мерам профилактики ВИЧ-инфекции[14].
Примечания[править]
- ↑ 1,0 1,1 Дудина Г.А., Мабудзаде Ч.К., Оганнисян А.А., Немыкин В.Н. ВИЧ-ассоциированные лимфомырус. // Креативная хирургия и онкология. — 2022. — том 12. — № 4. — С. 320-327. — DOI:10.24060/2076-3093-2022-12-4-320-327
- ↑ 2,0 2,1 2,2 Berhan A., Bayleyegn B., Getaneh Z. HIV/AIDS Associated Lymphoma: Reviewангл. // Blood Lymphat Cancer. — 2022. — том 12. — С. 31-45. — DOI:10.2147/BLCTT.S361320
- ↑ Khwaja J., Burns J.E., Ahmed N., Cwynarski K. HIV-associated lymphoma—advances in clinical managementангл. // Annals of Lymphoma. — 2021. — том 5. — ISSN 2616-2695. — DOI:10.21037/aol-21-16
- ↑ 4,0 4,1 4,2 4,3 Liu Y., Xie X., Li J. et al. Immune Characteristics and Immunotherapy of HIV-Associated Lymphomaангл. // Curr Issues Mol Biol. — 2024. — том 46. — № 9. — С. 9984-9997. — DOI:10.3390/cimb46090596
- ↑ 5,0 5,1 Wang C., Liu J., Liu Y. Progress in the Treatment of HIV-Associated Lymphoma When Combined With the Antiretroviral Therapiesангл. // Front Oncol. — 2022. — том 11. — С. 798008. — DOI:10.3389/fonc.2021.798008
- ↑ Пивник А. В., Пархоменко Ю. Г., Криволапов Ю. А. и др. Соматические проблемы ВИЧ-медицины: СПИД-ассоциированные лимфомы // Онкогематология. — 2007. — № 3.
- ↑ Xiong Y., Liu W., Chen X. et al. Survival of HIV associated diffuse large B-cell lymphoma and Burkitt lymphoma in Chinaангл. // Sci Rep. — 2024. — том 14. — С. 30397. — DOI:10.1038/s41598-024-80749-9
- ↑ P.T. Naing, A. Kaur, D. T. Lynch Burkitt Lymphomaанглйиский. Statpearls (February 17, 2025.). Проверено 11 мая 2025.
- ↑ H. Kaseb, H. M. Babiker. Hodgkin Lymphomaанглийский. Statpearls (June 26, 2023). Проверено 11 мая 2025.
- ↑ Gathers D.A., Galloway E., Kelemen K. et al. Primary Effusion Lymphoma: A Clinicopathologic Perspectiveангл. // Cancers (Basel). — 2022. — том 14. — № 3. — С. 722. — DOI:10.3390/cancers14030722
- ↑ Попова М.О., Цыганков И.В., Гудожникова Я.В. и др Плазмобластная лимфома у пациентов с ВИЧ-инфекцией: обзор литературы и результаты российского многоцентрового ретроспективного исследованиярус. // Клиническая онкогематология. Фундаментальные исследования и клиническая практика. — 2022. — том 15. — № 1. — С. 28-41. — DOI:10.21320/2500-2139-2022-15-1-28-41
- ↑ 12,0 12,1 Lebrun L., Allard-Demoustiez S., Salmon I. Pathology and new insights in central nervous system lymphomasангл. // Curr Opin Oncol. — 2023. — том 35. — № 5. — С. 347-356. — DOI:10.1097/CCO.0000000000000978
- ↑ S. Gandhi. Diffuse Large B-Cell Lymphomaанглийский. Medscape (Nov 04, 2025). Проверено 11 мая 2025.
- ↑ 14,0 14,1 14,2 14,3 Национальная вирусологическая ассоциация., Московское онкологическое общество ВИЧ-инфекция у взрослыхрусский. Министерство Здравоохранения Российской Федерации (22.07.2024). Проверено 5 ноября 2025.
- ↑ Glushko T., He L., McNamee W., Babu A.S., Simpson S.A. HIV Lymphadenopathy: Differential Diagnosis and Important Imaging Featuresангл. // Am J Roentgenol. — 2021. — том 216. — № 2. — С. 526-533. — DOI:10.2214/AJR.19.22334
Литература[править]
- Дудина Г.А., Мабудзаде Ч.К., Оганнисян А.А., Немыкин В.Н. ВИЧ-ассоциированные лимфомырус. // Креативная хирургия и онкология. — 2022. — том 12. — № 4. — С. 320-327. — DOI:10.24060/2076-3093-2022-12-4-320-327
- Berhan A., Bayleyegn B., Getaneh Z. HIV/AIDS Associated Lymphoma: Reviewангл. // Blood Lymphat Cancer. — 2022. — том 12. — С. 31-45. — DOI:10.2147/BLCTT.S361320
- Liu Y., Xie X., Li J., Xiao Q., He S., Fu H., Zhang X., Liu Y. Immune Characteristics and Immunotherapy of HIV-Associated Lymphomaангл. // Curr Issues Mol Biol. — 2024. — том 46. — № 9. — С. 9984-9997. — DOI:10.3390/cimb46090596
Одним из источников, использованных при создании данной статьи, является статья из википроекта «Рувики» («ruwiki.ru») под названием «СПИД-ассоциированная лимфома», расположенная по адресу:
Материал указанной статьи полностью или частично использован в Циклопедии по лицензии CC-BY-SA 4.0 и более поздних версий. Всем участникам Рувики предлагается прочитать материал «Почему Циклопедия?». |