Саркопсиллёз
Саркопсиллёз, или тунгиоз (лат. Sarcopsyllosis, Tungiasis, также известный как «Nigua»[1]«Pio and bicho de pie»[1], «Pique»[1]) — тропическая паразитарная болезнь из группы дерматофилиазов, характеризующаяся зудом и болями в поражённых участках кожи, образованием крупного воспалительного инфильтрата в месте внедрения паразита[2].
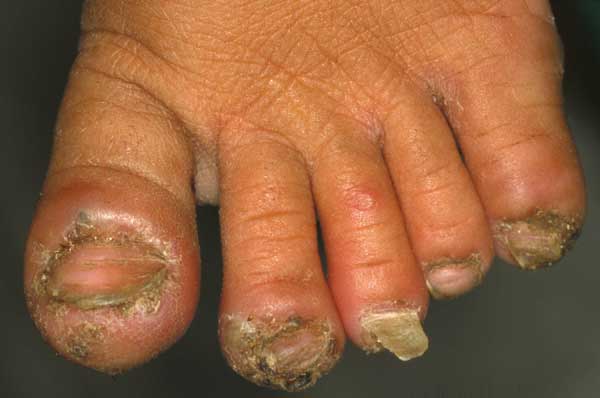
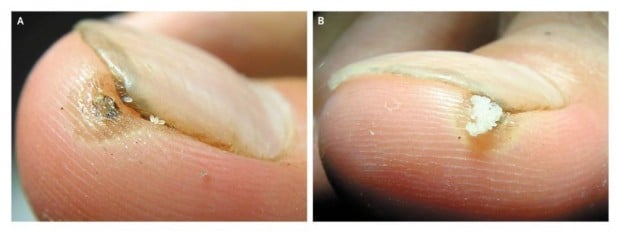
Болезнь вызывается самкой мелких (ширина тела около 1 мм) блох рода Tunga[3], обитающих в тропических районах Африки, Карибского бассейна, Центральной и Южной Америки и Индии. Тунгиоз вызывает воспаление кожи, сильную боль, зуд и ранку в очаге инфекции. Опухшая красная ранка имеет чёрную точку в центре и окружена белым ореолом. Также всегда отмечается шелушение кожи, особенно после того, как блоха расширяется при гипертрофии.
Болезнь представляет особую проблему для общественного здравоохранения в эндемичных для данного заболевания районах, таких как Нигерия, Тринидад, Тобаго и Бразилия, где его распространённость, особенно в бедных общинах, иногда достигает 50 %[4].
История[править]
По некоторым данным, в Перу тунгиоз, вызываемый Tunga trimamillata, встречался в течение 14 веков[5].
Однако первый задокументированный случай саркопсиллёза относится к 1526 году, когда Гонсало Фернандес де Овьедо-и-Вальдес описал симптомы болезни у членов экипажа каравеллы «Санта-Мария» из экспедиции Христофора Колумба, после того, как они потерпели крушение на Гаити[6][7]. Гонсало Фернандес де Овьедо-и-Вальдес также сообщил, что в некоторых странах Южной и Центральной Америки жители были вынуждены покинуть свои деревни из-за этих блох[8]. Позднее Карл Линней описал блоху Tunga penetrans[5].
Вместе с кораблями мореплавателей вызывающая саркопсиллёз блоха распространилась по всему миру. Так, распространение заболевания в большей части Африки происходило с XVII по XIX век, в частности, в 1873 году, когда инфицированные члены экипажа судна «Томас Митчелл» занесли его в Анголу из Бразилии[9][10].
Этиология[править]
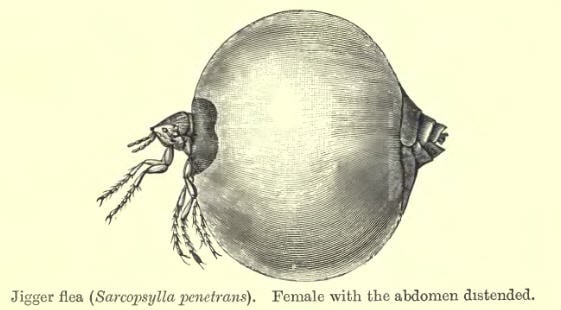
Возбудитель — песчаная (земляная) блоха Tunga penetrans (Linnaeus, 1758), syn. Sarcopsylla penetrans из семейства Hectopsyllidae отряда Siphonaptera. Эти блохи способны прыгать на высоту 15—35 см. Блохи обитают в тропиках в земляном полу хижин и хлевов. Длина тела половозрелого самца — 1 мм.
Самец кусает и сосёт кровь людей и животных как обычная блоха[11]. Оплодотворённая самка же внедряется в эпидермис кожи (обычно под ногти рук или ног или между пальцами) и является внутрикожным эндопаразитом. Брюшко паразита растёт, и самка через 5—6 дней после внедрения становится размером с горошину. В ней созревает несколько сотен яиц. Ткани вокруг воспаляются, образуются язвы. Блоха «выстреливает» яйца из ранки, после чего может оттуда выползти.
Из яйца (средняя длина — 0,6 мм) через 2—4 дня выходит безногая личинка. Только вылупившиеся личинки на первой стадии роста имеют среднюю длину 1,5 мм. На второй и последней стадии (Tunga penetrans является уникальной среди блох в том, что она имеет только две стадии вместо трёх) личинки уменьшается в размерах до 1,15 мм после роста, по крайней мере, до 2,9 мм. Развитие от стадии 1 до стадии 2 длится менее одного дня[12]. На 11—20-й день личинка превращается в куколку, а ещё через 11 дней — во взрослую особь.
Личинки паразита живут на земляном полу, в сухих песчаных почвах, в тенистых уголках пляжей. Они питаются органическими веществами, через 3 недели окукливаются и затем превращаются во взрослых блох[13].
Эпидемиология[править]
Поскольку самки несут от 100 до 200 яиц, переносчиками являются сами заражённые особи, распространяющие яйца на других млекопитающих. Кроме человека, Tunga penetrans поражают свиней, собак, кошек, крупный рогатый скот, овец, лошадей, мулов, ослов, обезьян, слонов, крыс, мышей и других животных[14].
Важным резервуаром инфекции (по данным исследований в Нигерии) являются свиньи (заражённость в очагах до 54,8% и даже 83%), собаки (заражённость в очагах до 45,5%), что отражает огромное значение заболевания для ветеринарии. Также широко поражены синантропные грызуны: чёрная крыса Rattus rattus (заражённость в очагах до 29,4%) и домовая мышь Mus minutoides (заражённость в очагах до 15,4%)[15].
Чаще болеют люди, не носящие обуви. Мужчины болеют чаще женщин. В основном, болезнью поражены бедные слои населения. Пик заболеваемости приходится на сентябрь, минимум — на январь[16].
Саркопсиллёз иногда смешивают с тромбидиазом из-за схожести английских названий возбудителей — «Chigger bite» (краснотелковые клещи, возбудители тромбидиаза) и «Chigoe flea» (блоха Tunga penetrans, возбудитель саркопсиллёза) (и соответственно одинаково называют болезнь Chiggers/Jiggers), а также некоторых общих симптомов поражения кожи (зуд и т. д.).
Реже (в Эквадоре и Перу) тунгиоз вызывает другой вид блох из рода Tunga — Tunga trimamillata (Pampiglione et al., 2002)[17]. Кроме человека, данная блоха является патогенной для коз, овец, коров, свиней[18].
В наше время саркопсиллёз — частое заболевание кожи ног жителей тропиков, особенно в Африке, на Мадагаскаре, в тропической Америке, Гаити, на западном побережье Индии, в Пакистане (на 2009 год, тунгиоз был описан в 88 странах мира)[19]. В Европе, США, Израиле[20] и в России известны завозные случаи тунгиоза у туристов. В эндемичных очагах, в бедной среде Нигерии, Тринидада, Тобаго и Бразилии заражённость населения может достигать 50—76 %[4]. Заражённость не зависит от расы, мужчины поражаются чаще и сильнее, чем женщины, в зависимости от страны, пик заражённости варьируется у разных возрастов[19].
Жители не эндемичных стран заболевают когда прибывают в качестве туристов и или по работе в страны, где распространена данная инфекция.
Эпидемии тунгиоза[править]
Описаны эпидемии тунгиоза, например в Уганде в 2010 году, где заразилось около 20 тысяч человек, из которых более 20 погибло[21][22]. Во время вспышки тунгиоза в Медоре на Гаити заболело 1125 человек, из них погибло 127 человек[23].
Клиническая картина и патогенез[править]
Инкубационный период при саркопсиллёзе составляет от 8 до 12 дней. Различают 5 стадий тунгиоза:
- проникновение паразита на кожу;
- внедрение в кожу;
- блоха разбухает и откладывает яйца;
- самка блохи начинает погибать;
- симптомы, остающиеся после гибели паразита, процесс заживания[24].
Поражается кожа стопы (чаще всего под ногтями; на ноги приходится большая часть случаев локализации паразита), спины, затылка, запястья, рук, локтей, в области лодыжек, колен, бёдер, ягодичной области, лобка, шеи, живота, а также может поражаться паховая область, губы, веко, яички, половой член[25][26]. При низкой (мягкой) инвазии очагов поражения не более 5, при средней (умеренной) — от 6 до 30, при тяжёлой — более 30. Тяжёлая форма чаще встречается у пожилых людей[27] (может быть более 120 паразитарных очагов), у маленьких детей (описаны случай, когда у детей обнаруживали 90−96 паразитарных очагов)[28].
Внедрившиеся в кожу самки блохи с помощью ферментов разъедают поверхность кожи и проникают под неё, где развиваются до размеров горошины и погибают, вызывая тяжёлый зуд, сильную боль, воспаление, волдырь, фурункул, язву, пустулы, папулы, отёк и нередко изъязвление (реакции на ферментную жидкость паразита). Бессонница.
Иммунологический ответ на внедрение паразита — воспалительная реакция — начинается в виде эритемы. Вокруг внедрившегося паразита развивается воспалительный инфильтрат с исходом в нагноение. Паразит питается кровью из сосудов сосочкового слоя дермы. Созревшие яйца выделяются самкой по одному из отверстия на конце брюшка в течение 7—10 дней. После откладки яиц (общим числом около 150—200 шт.) паразит погибает. Разбухание самки и давление отложенных ею яиц вызывают сдавливание соседних нервов и кровеносных сосудов.
Внедрившаяся в кожу блоха сообщается с воздухом с помощью отверстия в коже диаметром около 250—500 мкм, через которое она вместе с яйцами дышит, выделяет яйца и выбрасывает фекалии, поэтому из ранки, кроме яиц, выделяется жидкость, состоящая из продуктов обмена и распада паразита.
Некоторые заболевшие не могут работать и даже ходить из-за боли. Если паразит локализован на ноге, боль усиливается ночью и при ходьбе .
Биопсия выявляет образование микроабсцессов в коже, гиперкератоз (чрезмерное развитие рогового слоя кожи), акантоз (утолщение роткового слоя эпидермиса), паракератоз (нарушение ороговения клеток эпидермиса), гипергранулёз (утолщение зернистого эпидермиса в результате увеличения числа рядов клеток), спонгиоз (межклеточный отёк), папилломатоз (образование бородавок) и геморрагическую область в дерме. Наблюдаются также паразит и овальные белые яйца[29].
Редкая инвазия в паховую область характеризуется гиперплазией, наблюдается псевдоэпителиома эпидермиса, образование экзофитных опухолей до 3 см в диаметре, напоминающих бородавки[30].
Описан случай тунгиоза языка у женщины в Уганде[31].
Осложнения[править]
Осложнения тунгиоза, как правило, связаны с возникновением вторичной инфекции, которая может привести к развитию абсцесса, бактериемии. Известны случаи, когда вторичные инфекции (гангрена, столбняк) приводили к гибели людей, заражённых песчаными блохами.
Микробы попадают в ранку вследствие нарушения целостности кожи паразитом, расчёсов и переносятся непосредственно самой блохой. Так как внедрившаяся блоха питается кровью из субэпидермальных кровеносных сосудов, в процесс подключаются внешняя поверхность кожи и системный кровоток.
Осложнения при тунгиозе способны вызывать около 150 патогенных микроорганизмов, включая золотистого стафилококка и Wolbachia endobacteria[32][33][34].
Вторичную инфекцию также могут обусловить попытки самостоятельного лечения с помощью нестерильных инструментов.
В результате патологий, вызванных паразитом или микроорганизмами, возможны деформация пальцев, самоампутация пальца, деформация и потеря ногтей, лимфостаз, лимфангит, некроз тканей, сепсис, пневмония, целлюлит, тромбофлебит, лимфатический отёк, глубокое изъязвление, вплоть до костей.
Тунгиоз может взаимно осложнять другие тропические паразитарные болезни — слоновость ног (см. Филяриатозы) и пр.
Лечение и профилактика[править]
Дифференциальный диагноз проводят, чтобы отличить саркопсиллёз от других внутрикожных паразитов, пуликоза, укусов клещей, чесотки, миграций личинок гельминтов в коже (см. larva migrans), дракункулёза.
Инвазия Tunga penetrans может также имитировать глубокие микозы, бородавки, инородные тела и наркотизирующий васкулит. Атипичный тунгиоз дифференцируется с псевдоэпителиомой, остроконечными кондиломами и кожным туберкулёзом. Иногда приходится дифференцировать с хромобластомикозом и кожным лейшманиозом.
Диагноз ставят на основании данных анамнеза (посещение или проживание в очаге саркопсиллёза), клинической картины, обнаружения паразита.
Лечение хирургическое: блоху осторожно, с соблюдением асептики, пинцетом или стерильной иглой полностью извлекают из кожи, рану дезинфицируют и накладывают на неё повязку. Предварительно блоху можно убить хлороформом. Для предотвращения и терапии вторичной инфекции применяют антибиотики: флюклоксациллин, коамоксиклав, триметоприм, сульфаметоксазол, метронидазол или эритромицин[35]. Необходима профилактика столбняка.
Прогноз при оказании адекватной медицинской помощи обычно благоприятный, однако при развитии вторичной инфекции возможен летальный исход.
Профилактика саркопсиллёза — борьба с блохами и защита от их укусов, ношение носков и обуви; воздержание от лежания и сидения голым телом на земле; поддержание чистоты в доме, мытьё ног в тёплой воде после прогулки по заражённой местности[36].
См. также[править]
Видеогалерея[править]
Болезненный процесс избавления от паразитов
| Jiggers causing misery for Kenyans
|
Tungiasis in villagers of Maseno, Kenya
| NewSpring Foot-washing/Jigger Removal
|
Epidemia de pulgas na Orla Lagunar
| Jigger Documentary
|
Источники[править]
- ↑ 1,0 1,1 1,2 Dermatology: 2-Volume Set. — St. Louis: Mosby, 2007. — ISBN 1-4160-2999-0.
- ↑ Саркопсиллёз. М.: Медицинская энциклопедия. (1991—96 гг). — Малая медицинская энциклопедия. Проверено 29 сентября 2011.
- ↑ Veraldi S, Valsecchi M. Imported tungiasis: a report of 19 cases and review of the literature.English // Int J Dermatol.. — 2007. — В. 10. — том 46. — С. 1061—6. — PMID 17910715.
- ↑ 4,0 4,1 Heukelbach, Jorg. «Invited Review — Tungiasis.» Revista do Instituto de Medicina Tropical de São Paulo 47.6 (2005): 307—313
- ↑ 5,0 5,1 Evidence of Tungiasis in Pre-Hispanic America
- ↑ Darmstadt GL, Francis JS (May 2000). «Tungiasis in a young child adopted from South America». Pediatr. Infect. Dis. J. 19 (5): 485–7. DOI:10.1097/00006454-200005000-00024. PMID 10819355.
- ↑ Darmstadt GL, Francis JS (May 2000). «Tungiasis in a young child adopted from South America». Pediatr. Infect. Dis. J. 19 (5): 485-7. doi:10.1097/00006454-200005000-00024. PMID 10819355.
- ↑ Tungiasis in The United States: A travel souvenir
- ↑ Joseph JK, Bazile J, Mutter J, Shin S, Ruddle A, Ivers L, Lyon E, Farmer P. Tungiasis in rural Haiti: a community-based response.English // Trans R Soc Trop Med Hyg.. — 2006. — В. 10. — том 100. — С. 970—4. — PMID 16516941.
- ↑ Hoeppli R. Early references to the occurrence of Tunga penetrans in tropical Africa.English // Acta Trop.. — 1963. — том 20. — С. 143—53. — PMID 13963854.
- ↑ Blood-feeding of Tunga penetrans males
- ↑ Nagy N, Abari E, D’Haese J, Calheiros C, Heukelbach J, Menche N, Feldmeier H, Mehlhorn H «Investigations on the Life Cycle and Morphology of Tunga penetrans in Brazil.» Parasitology Research 101.Supplement 2 (2007): 233—242. Springer-Verlag, 2007. SpringerLink. 22 Feb. 2009
- ↑ Тунгиоз (tungiasis, саркопсиллез)
- ↑ Dermatologic Manifestations of Tungiasis
- ↑ Pigs are the most important animal reservoir for Tunga penetrans (jigger flea) in rural Nigeria
- ↑ SEASONAL VARIATION OF TUNGIASIS IN AN ENDEMIC COMMUNITY
- ↑ Pampiglione S, Trentini M, Fioravanti ML, Gustinelli A (March 2004). «Differential diagnosis between Tunga penetrans (L., 1758) and T. trimamillata Pampiglione et al., 2002 (Insecta, Siphonaptera), the two species of the genus Tunga parasitic in man». Parasite 11 (1): 51–7. PMID 15071827. Проверено 2011-09-19.
- ↑ On a new species of sand flea from Ecuador and tungiasis, a problem of Public Health in many developing countries
- ↑ 19,0 19,1 Smith, Darvin Scott Tungiasis: epidemiologyEnglish. Emedicine. Архивировано из первоисточника 31 января 2012. Проверено 2 октября 2011.
- ↑ A case of tungiasis in Israel
- ↑ Эпидемия тунгиоза в Уганде - 20 погибших
- ↑ Эпидемия тунгиоза в Уганде
- ↑ Tungiasis Epidemic in Medor
- ↑ Eisele M, Heukelbach J, Van Marck E, Mehlhorn H, Meckes O, Franck S, Feldmeier H. «Investigations on the biology, epidemiology, pathology and control of Tunga penetrans in Brazil: I. Natural history of tungiasis in man .» Parasitology Research 90.2 (2003): 87—99. Springer-Verlag, 2003. SpringerLink. 22 Feb. 2009
- ↑ An unusual case of ectopic tungiasis with pseudoepitheliomatous hyperplasia
- ↑ ECTOPIC LOCALIZATION OF TUNGIASIS
- ↑ Risk Factors for Tungiasis in Nigeria: Identification of Targets for Effective Intervention
- ↑ Severe Tungiasis in Underprivileged Communities: Case Series from Brazil
- ↑ An Ectopic Case of Tunga spp. Infection in Peru
- ↑ An unusual case of ectopic tungiasis with pseudoepitheliomatous hyperplasia
- ↑ Tungiasis presenting as a soft tissue oral lesion
- ↑ Heukelbach, Jorg. Tungiasis. Sept. 2004. Orphanet.com. 23 Feb. 2009 http://www.orpha.net/data/patho/GB/uk-Tungiasis.pdf
- ↑ Fischer P, Schmetza C, Bandib C, Bonowa I, Manda S, Fischera K, Büttner D. Experimental Parasitology 102.3-4 (2002): 201—211. Science Direct. 23 Feb. 2009 Tunga penetrans: molecular identification of Wolbachia endobacteria and their recognition by antibodies against proteins of endobacteria from filarial parasites. Copyright © 2003 Elsevier Science
- ↑ Feldmeier, H, Heukelbach J, Eisele M, Souza A, Barbosa L, Carvalho C. «Bacterial superinfection in human tungiasis.» Tropical Medicine & International Health 7.7 (2002): 559—564. Wiley InterScience. 23 Feb. 2009
- ↑ J. Joseph, J. Bazile, J. Mutter, S. Shin, A. Ruddle, L. Ivers, E. Lyon, P. Farmer. «Tungiasis in rural Haiti: a community-based response.» Transactions of the Royal Society of Tropical Medicine and Hygiene 100.10 (2006): 970—974. 22 Feb. 2009
- ↑ Tungiasis is an infestation